グンゼ株式会社は、糖尿病性足潰瘍(DFU)または慢性静脈不全(VLU)による難治性潰瘍を対象としたヒト由来の羊膜使用組織治癒促進用材料 「EPIFIX(R)、以下、エピフィックス」 を、2023年2月1日から、連結子会社であるグンゼメディカル株式会社より、販売を開始します。
販売開始に至った経緯
エピフィックスは、外国特例承認制度により、2021年6月7日付、外国製造業者であるMiMedx Group, Inc.が、EPJメディカルサービス株式会社を通じて、医療機器の製造販売承認を取得しました。そして、2022年9月1日付、保険償還価格を取得(新設)しました。
この商品は、日本初のヒト羊膜使用組織治癒促進用材料であり、創傷領域分野の医療機器で豊富な実績と経験を持つグンゼメディカル株式会社を総代理店として、協働で商品の市場普及を進めることとなりました。
羊膜使用組織治癒促進用材料 「エピフィックス」の特長
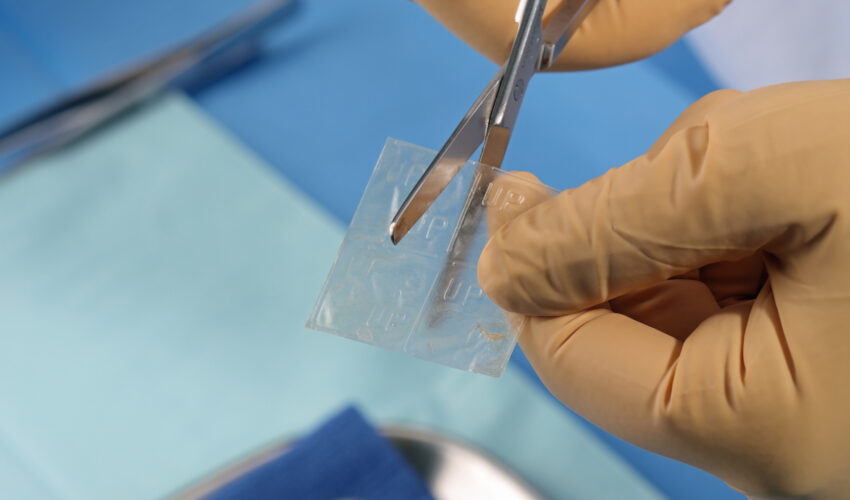
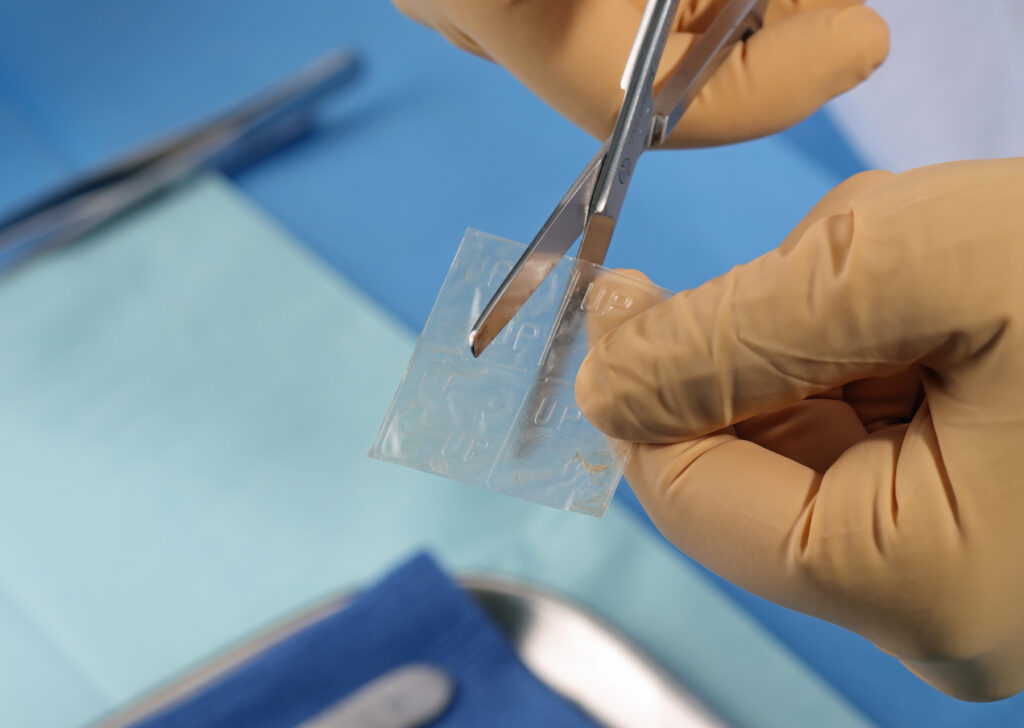
エピフィックスは、MiMedx社独自の加工方法「PURION(R)プロセス」(特許取得)により加工・乾燥したヒト胎盤の羊膜・絨毛膜で、ヒト胎盤由来の成分を含有しています。羊膜・絨毛膜はコラーゲン性の膜で、細胞外マトリックス(extracellular matrix:ECM)タンパク質、増殖因子、サイトカインなど300種以上の調整たんぱく質を含有しているため、瘢痕組織形成の低減、炎症の抑制ならびに創傷治癒の促進に寄与します。
対象疾患としては、従来の治療法では反応しない難治性の糖尿病性足潰瘍および静脈性下肢潰瘍の治療機器として承認されています。創傷領域における日本初のヒト羊膜製品となります。
米国では既に200万枚の製品が販売されており、米国市場においてはヒト胎盤由来組織製品に関してトップシェアを誇っています。保険適用条件として、通常のケアを4週間以上施行しても創面積が50%以上縮小しないものであること、導入時には入院管理下で使用すること、治療開始から12週まで、一連の治療計画につき224㎠を限度とすること、また、フットケア・足病医学会主催のエピフィックス講習会を受講した医師が所属していること等が定められています。